Radiocarbon (14C) Dating
การตรวจหาอายุด้วยคาร์บอนกัมมันตรังสี (radiocarbon dating) เป็นเทคนิคการหาอายุที่ใช้ไอโซโทปคาร์บอน-14 (carbon-14 หรือ 14C) ซึ่งเป็นไอโซโทปรังสีในธรรมชาติ และมีอยู่ในสิ่งมีชีวิต ซึ่งขณะมีชีวิตอยู่จะดูดกลืนคาร์บอน-14 ในรูปคาร์บอนไดออกไซด์มีสัดส่วนคงที่ เมื่อสิ่งมีชีวิตตายลงก็จะไม่สามารถรับคาร์บอน-14 ได้อีกต่อไป และปริมาณคาร์บอน-14 ในซากสิ่งชีวิตจะลดลงเรื่อยๆ ที่เกิดขึ้นจากการสลายตัว (decay) ด้วยอัตราคงที่ ไม่ขึ้นอยู่กับการเปลี่ยนแปลงอุณหภูมิ ความดัน และปฏิกิริยาทางเคมี โดยเวลาที่ธาตุกัมมันตรังสีใช้ไปในการสลายตัวจนมีปริมาณเหลือเป็นครึ่งหนึ่งของปริมาณที่มีอยู่เดิม เรียกว่า ครึ่งชีวิต (half-life) โดยค่าครึ่งชีวิตของคาร์บอน-14 เท่ากับ 5730 ปี ตัวอย่างเช่น ถ้ามีปริมาณคาร์บอน 1 กรัม หลังจากเวลาผ่านไป 5730 ปี จะเหลือปริมาณคาร์บอน-14 อยู่ 0.5 กรัม
การสลายตัวของธาตุกัมมันตรังสีสามารถเขียนในรูปสมการทางคณิตศาสตร์ ได้ดังนี้
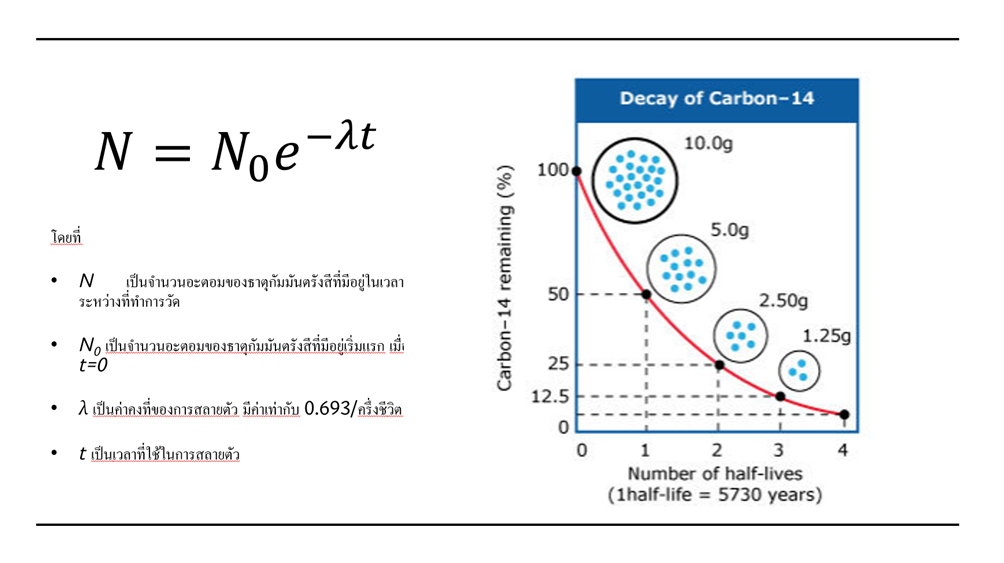
เมื่อนักวิทยาศาสตร์สามารถวัดปริมาณคาร์บอน-14 ที่คงเหลือในวัตถุได้ จึงสามารถนำค่าจากการวัดมาคำนวณหาค่าอายุของวัตถุที่สนใจได้
หลักการกำหนดค่าอายุโดยวิธีคาร์บอน-14
ธาตุคาร์บอนในธรรมชาติ ประกอบด้วย 3 ไอโซโทป คือ คาร์บอน-12 คาร์บอน-13 ซึ่งเป็นไอโซโทปเสถียร และคาร์บอน-14 หรือเรียกอีกอย่างหนึ่งว่าคาร์บอนกัมมันตรังสี (radiocarbon) เป็นไอโซโทปรังสี ที่เกิดจากปฏิกิริยานิวเคลียร์ ระหว่างอนุภาคนิวตรอนที่ได้มาจากรังสีคอสมิก กับอะตอมของธาตุไนโตรเจนในบรรยากาศชั้นบน เมื่อเกิดขึ้นแล้วเข้ารวมตัวกับออกซิเจนในบรรยายกาศ กลายเป็นแก๊สคาร์บอนไดออกไซด์ จากนั้นจึงแพร่ลงมายังบรรยากาศชั้นล่าง และถูกนำไปใช้ในกระบวนการสังเคราะห์แสงของพืชกลายเป็นสารอินทรีย์ที่มีคาร์บอน-14 และเมื่อสัตว์กินพืชก็จะได้รับสารอินทรีย์ที่มีคาร์บอน-14 เป็นองค์ประกอบในร่างกาย นอกจากนั้นคาร์บอน-14 ในชั้นบรรยากาศ เกิดจากแก๊สคาร์บอนไดออกไซด์รวมตัวกับน้ำ โดยอยู่ในรูปของคาร์บอเนต หรือไบคาร์บอเนต ในระบบน้ำบาดาล ปริมาณคาร์บอน-14 ต่อกรัมคาร์บอนในพืชหรือสัตว์ขณะมีชีวิตอยู่จะมีปริมาณเดียวกับปริมาณคาร์บอน-14 ต่อกรัมคาร์บอนในบรรบยากาศหรือในน้ำเวลาปัจจุบัน เพราะมีสมดุลคงที่ตลอดเวลา
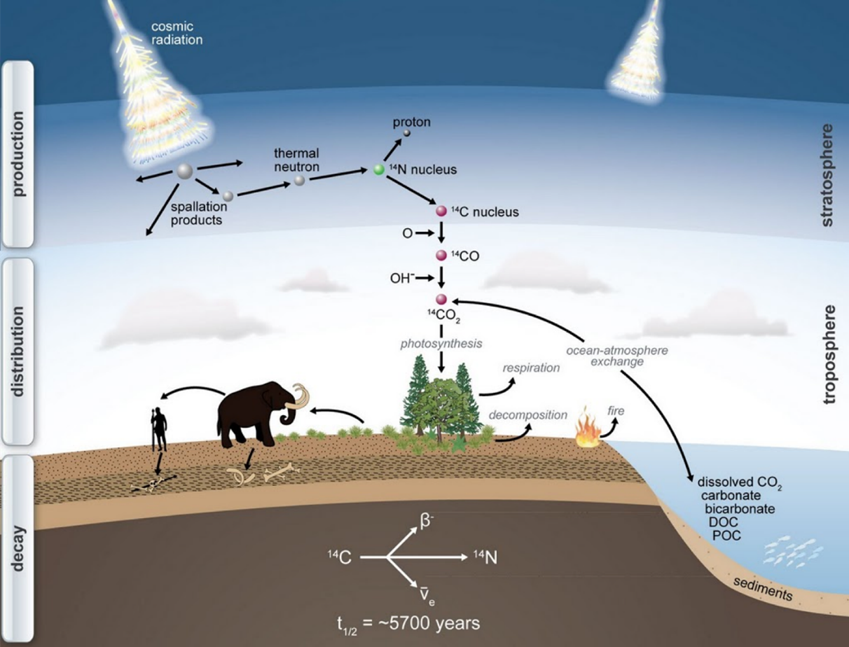
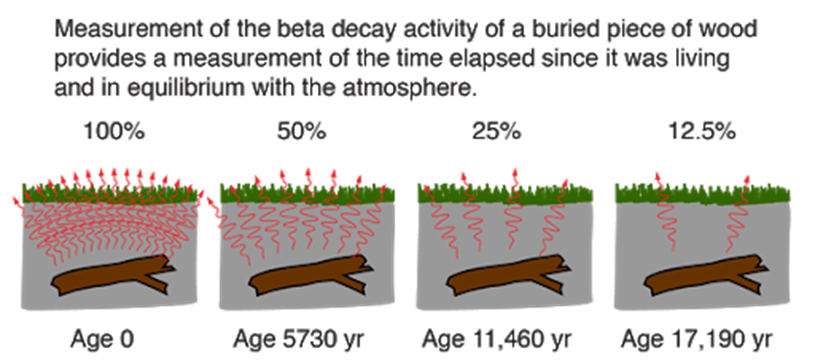
แต่เมื่อสิ่งมีชีวิตตายลง การแลกเปลี่ยนระหว่างคาร์บอน-14 ในตัวสิ่งมีชีวิต กับคาร์บอน-14 ในบรรยากาศหรือในน้ำจะสิ้นสุดลง ดังนั้นจึงส่งผลต่อปริมาณคาร์บอน-14 ที่มีอยู่แต่เดิมก็จะลดจำนวนลงไป ตามอัตราการสลายตัวของสารกัมมันตรังสี ที่นิยามว่า “ครึ่งชีวิต” (half-life) ดังนั้น ถ้าทราบถึงปริมาณคาร์บอน-14 ที่มีอยู่อย่างคงที่ในบรรยากาศและที่มีอยู่ปัจจุบันในตัวอย่างที่สนใจ ก็สามารถคำนวณหาเวลาที่ผ่านมาตั้งแต่ตัวอย่างนั้นตายไปจนถึงเวลาปัจจุบัน
การวิเคราะห์หาอายุของวัตถุซึ่งมีคาร์บอนเป็นองค์ประกอบ ต้องนำวัตถุหรือตัวอย่างที่สนใจมาผ่านกระบวนการเปลี่ยนคาร์บอนให้อยู่ในรูปสารประกอบต่าง ๆ เช่น คาร์บอนไดออกไซด์ (carbon dioxide) เบนซีน (benzene) หรือ แกรไฟต์ (graphite) จากนั้นวัดค่ากัมมันตภาพรังสีของคาร์บอน-14 โดยใช้เครื่องวัดรังสีแบบเรืองแสงในของเหลวระดับต่ำ (low level liquid scintillation counter) เปรียบเทียบกับค่ากัมมันภาพรังสีของสารอ้างอิงมาตรฐาน (reference standard) ซึ่งสารอ้างอิงมาตรฐานที่นิยมใช้อยู่ในปัจจุบัน ได้แก่ กรดออกซาลิก (oxalic acid) และ เอเอ็นยู ซูโครส (ANU sucrose) หรือการวัดปริมาณคาร์บอน-14 โดยตรง ด้วยเครื่องเร่งอนุภาค (accelerator mass spectrometry, AMS) เทคนิคการกำหนดค่าอายุด้วยคาร์บอน-14 นี้ สามารถกำหนดอายุได้ในช่วง 300 – 50,000 ปี


การรายงานผลการกำหนดค่าอายุ ด้วยวิธีคาร์บอน-14
แบ่งออกเป็น 2 รูปแบบ ได้แก่
- รายงานในรูปของ percent modern carbon (PMC)
- รายงานในรูปจำนวนปี year before present (Year, B.P.)
ปัจจัยที่ส่งผลต่อความคลาดเคลื่อนในการกำหนดค่าอายุ
- เนื่องจากค่าครึ่งชีวิตของคาร์บอน-14
- เนื่องจากการเปลี่ยนแปลงปริมาณคาร์บอน-14 ในบรรยากาศ
2.1 การเปลี่ยนแปลงของสนามแม่เหล็กโลก
2.2 การเปลี่ยนแปลงความเข้มข้นของรังสีคอสมิก
2.3 ผลจากการปฏิวัติอุตสาหกรรม
2.4 ผลจากการทดลองอาวุธนิวเคลียร์ในบรรยากาศ - เนื่องจากการปนเปื้อนของตัวอย่าง
- เนื่องจากการเกิดปฏิกิริยา Isotope fractionation
นายเกียรติพงษ์ คำดี : นักวิทยาศาสตร์นิวเคลียร์ชำนาญการพิเศษ
และ นางสาวนิชธิมา เอื้อพูนผล : นักวิทยาศาสตร์นิวเคลียร์
ฝ่ายเทคโนโลยีสิ่งแวดล้อม
ศูนย์วิจัยและพัฒนาเทคโนโลยีนิวเคลียร์
สถาบันเทคโนโลยีนิวเคลียร์แห่งชาติ (องค์การมหาชน)